安特罗肠病毒疫苗 传捷报

安特罗总经理张哲玮表示,近期将向越南提出药证申请,目标锁定东南亚各国新生儿市场,并布局进入大陆市场。图/安特罗提供
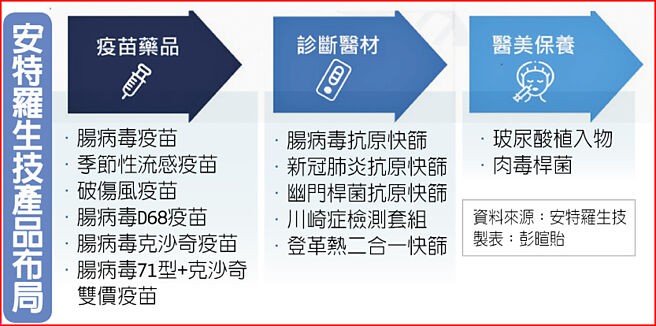
安特罗生技产品布局
安特罗生技2日宣布,安特罗肠病毒71型疫苗(EnVAX-A71)第三期临床试验疗效解盲达标,保护力数据高达99.12%,为目前全球市售肠病毒71型疫苗中保护力最高。安特罗肠病毒疫苗上市以来,逐步深耕小儿疫苗及检测市场,规划7月中旬向台湾证券交易所送件申请创新版上市。
安特罗总经理张哲玮表示,安特罗肠病毒71型疫苗去年取得食药署药证,以台湾流行的B4亚基因型病毒株,配合国光生技新一代高产能细胞培养生物反应器制程,并于台中潭子细胞厂建立新一代高产能细胞培养生物反应器制程,可提升安特罗肠病毒71型疫苗产能,明年起扩大供货。
为布局东南亚市场,安特罗已与越南国营最大疫苗公司VABIOTECH签订肠病毒71型疫苗销售合约,将向越南提出药证申请,锁定东南亚各国新生儿市场,并计划进军中国大陆市场。
安特罗肠病毒71型疫苗三期临床试验采多国多中心模式进行。台湾在中国医药大学附属医院、台大医院、台北荣总、林口长庚医院、台大新竹分院、台中荣总和彰化基督教医院等七家医学中心进行收案,共收案1,266人;越南则与越南巴斯德研究所合作,于槟知省和永隆省二家试验医院,完成2,727人收案,总收案有效样本数3,993人。
试验期间共追踪到肠病毒71型确诊个案71例(台湾2例、越南69例),其中疫苗组确诊个案数为1例,安慰剂对照组确诊数为70例,依「肠病毒疫苗临床研发策略指导原则」计算公式,疫苗有效性(VE)99.21%,并依Poisson回归统计分析后,95%信赖区间为94.31%~99.89%,其统计P值小于0.001,达到统计上显著意义。
张哲玮指出,2022年越南展开收案之际,正值一波肠病毒71型大流行,迅速累积阳性个案,解盲结果证明安特罗肠病毒疫苗安全性或保护力十分优异。
此外,安特罗和国家卫生研究院合作开发肠病毒克沙奇疫苗,目标三至五年内上市;也对全球第一款肠病毒71型抗原检测试剂、第二代肠病毒疫苗「A71+克沙奇二合一双价疫苗」展开部署。








