武汉生物40万支疫苗出包仅遭行政处罚 药监局:问题实属偶发
▲大陆假疫苗事件迄今仍不断延烧, 若武汉生物事件再扩大恐难以收拾。(图/路透社)大陆中心/综合报导 大陆国家药监局于8月1日,针对武汉生物百白破疫苗不合格事件解释道,「武汉生物该批次疫苗效价不合格主要原因,是分装设备短时间故障,导致待分装产品混悬液不均匀,属于偶发,中国食品药品检定研究院对企业有效期内的其他批次百白破疫苗进行抽样检验,检验结果符合规定」。
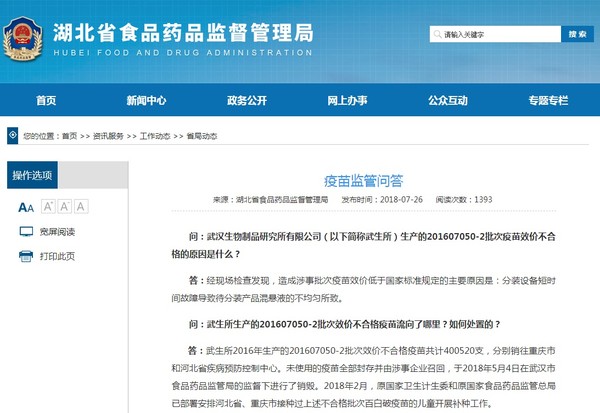
大陆药监局新闻发言人指出,原国家食品药品监督管理总局(简称食药监局),要求地方食品药品监督管理部门对武汉生物依法规、按程序进行处罚,故而武汉市食品药品监督管理局依照《药品管理法》相关法规,对武汉生物做出没收违法所得和罚款的行政处罚决定。▼湖北食药监局在7月26日即张贴公告公布武汉生物疫苗不合格的原因。(图/翻摄自湖北食药监局官网)
大陆药监局指出,在2017年时原食药监局的中国食品药品检定研究院,就在国家药品抽检中发现,武汉生物生产批号为201607050-2的百白破疫苗中的百日咳效价指标,不符合标准规定,并且相关资料都已在同年11月3日向社会公布,而且经现场检查和分析,武汉生物该批次疫苗效价不合格的主要原因是分装设备短时间故障,导致待分装产品混悬液不均匀,属于偶发。
药监局也解释,在发现效价不合格后,原食药监局即派出检查组对武汉生物进行全面现场检查,并会同原国家卫生计生委(国家卫生和计划生育委员会)部署,做好不合格百白破疫苗处置工作,同时湖北省食品药品监督管理局也进驻武汉生物,要求企业及时封存和召回不合格疫苗。
各单位多方经查后,发现该批不合格疫苗共计400520支,销往重庆市疾病预防控制中心190520支,销往河北省疾病预防控制中心210000支,经通知后武汉生物已召回全部未使用的疫苗,并于2018年5月4日在武汉市食品药品监督管理局的监督下进行了销毁。▼许多大陆民众现在都对长春长生生物和武汉生物的疫苗持保守态度,图为长春长生企业外观。(图/CFP)
药监局强调,武汉生物之后按着要求,已经允诺加强关键工艺设备的维保工作、保证设备正常运行、修订分装规程、加强分装过程品质控制、加强人员培训、提高人员品质意识等措施,以确保品质管制体系有效运行。
中国食品药品检定研究院经此后,再对武汉生物于有效期内的其他批次百白破疫苗进行抽样检验,检验结果符合规定,接着在随后批签发工作中,对该企业连续生产的30批百白破疫苗效价进行检测,结果也都全部符合规定。
药监局对外表示,在中国食品药品检定研究院之后,药监局也再次派出检查组,对武汉生物百白破疫苗整改情况进行检查,结果显示企业已经完成整改,符合药品生产品质管制规范(药品GMP)。











